Nanomalzemelerin 1–100 nm aralığındaki boyutları; yüksek yüzey alanı, yüzey reaktivitesi ve özgün biyolojik etkileşimleri
Nanomalzemelerin 1–100 nm aralığındaki boyutları; yüksek yüzey alanı, yüzey reaktivitesi ve özgün biyolojik etkileşimleri nedeniyle boyuta bağlı toksisite paternleri oluşturur. İşyeri hekimliği açısından maruziyetin ölçümü ve yönetimi, çok metrikli ölçüm, kontrol hiyerarşisi ve ihtiyat ilkesi ile yürütülmelidir. Bu yazıda uluslararası tanımlar (AB/ECHA nanoform), WHO/NIOSH/OECD rehberleri ve Türkiye’de KKDİK/SEA bağlamında güncel durumu özetlenmekte; ölçüm belirsizlikleri ve sağlık gözetimi için pratik öneriler sunulmaktadır.
GİRİŞ
Nanomalzemeler bilim ve teknolojiye umut vadeden ilerlemeler getirmeye devam etmekte ancak bununla birlikte, uygun şekilde tanımlanmalarını ve değerlendirilmelerini sağlamak için artan düzenleyici denetim gerekliliği de ortaya çıkmaktadır. Bu gereklilik ise, nanomalzeme tanımları hakkında kapsamlı tartışmalara yol açmaktadır. Çeşitli hükümet, endüstri ve standart kuruluşları tarafından nanomalzemeler için çok sayıda tanım önerilmiştir. Bu tanımlar genellikle unsurları ve kapsamları bakımından tutarsızdır; bu da bir malzemenin “nanomalzeme” olarak kabul edilip edilmediğinin belirlenmesinde kafa karışıklığına yol açabilir ve nanoteknoloji algısı üzerinde olumsuz etkiler yaratabilir.
Nanomalzemelerin tanımları ve bunların düzenleyici değerlendirmelerde kullanımı aktif bir bilimsel ve politik tartışma alanı olmuştur ve olmaya devam etmektedir (ICCA, 2010; Maynard, 2011; Stamm, 2011; Bleeker ve diğerleri, 2013).
Nanomalzemeler, nano olmayan formlarından farklı özellikler sergileyebilir, bu farklı özellikler, potansiyel insan sağlığı ve çevresel riskler hakkında soruları gündeme getirmiştir. Uluslararası Standardizasyon Örgütü (ISO), “nanomalzeme”yi “herhangi bir dış boyutu nano ölçekte olan veya iç yapısı veya yüzey yapısı nano ölçekte olan bir malzeme” (ISO, 2010) ve “nanoparçacık”ı ise “üç dış boyutu da nano ölçekte olan bir nano nesne” olarak tanımlamıştır; burada nano ölçek,yaklaşık 1-100 nm boyut aralığı olarak tanımlanmıştır (ISO, 2008). Sadece boyuta dayalı bu teknik tanımlar, risk değerlendirmesi açısından yetersiz olabilir çünkü bir nanomalzemenin ek incelemeye ihtiyaç duyup duymadığını belirlerken dikkate alınması gereken diğer önemli unsurları içermezler. Nanomalzemeler için bir tanım geliştirme konusundaki tartışmalar, iki farklı hususu karşılama gerekliliği nedeniyle zorlu olmuştur.
Tanım, ek değerlendirme gerektirebilecek malzemeleri tanımlayacak kadar geniş olmalı, ancak insan sağlığını veya çevreyi koruma açısından ek inceleme veya değerlendirmenin anlamlı olmayacağı malzemeleri içerecek kadar geniş olmamalıdır.
İnsanların ve çevrenin sağlığını ve güvenliğini en etkili şekilde korumak için kaynakların uygun şekilde tahsis edilmesini sağlamak için bir denge gereklidir. Bugüne kadar önerilen tanımlar, uygun bir denge kurma girişiminde çeşitli yaklaşımlar benimsemiştir, ancak belirli yargısal zorunlulukları karşılayabilirlerken, sıklıkla çelişkili içerme ve dışlama maddeleri, nanomalzemeler ve bunları içeren ürünlerin üreticileri için karmaşık bir düzenleyici labirent oluşturmaktadır. Çelişkili nanomalzeme tanımlarına ve potansiyel düzenlemelere uymaya çalışmanın getirdiği zorluklar uluslararası ticareti engelleyebilir ve daha da önemlisi, düzenleyici korumaların yeterliliğine olan kamu güvenini azaltabilir. Nanomalzemeler ne doğası gereği tehlikeli ne de doğası gereği güvenlidir (Auffan vd., 2009; Donaldson ve Poland, 2013) ve değerlendirme programlarında bu şekilde ele alınmamaları gerektiği yaygın olarak kabul edilmiştir (SCENIHR, 2007; Holdren, 2011; Hamburg, 2012).
Nanomalzemeleri Tanımlamanın Temel Unsurları
1.Boyut
Boyut, tüm nanomalzemelerin temel tanımlayıcı özelliğidir.Boyut anlaşılması kolay bir kavram olsa da,uygulaması daha zordur çünkü “nanometre ölçeğini” belirleyen doğal fiziksel veya kimyasal sınırlar yoktur.Geleneksel olarak, nanomalzemelere atıfta bulunmak için en yaygın kullanılan boyut aralığı 1-100 nm’dir, ancak kimyasal veya biyolojik bir perspektiften nanometre ölçeğini açıkça ayıran net bir çizgi yoktur.
Aralığın alt ucunda, 1 nm, bireysel moleküller ve nanomalzemeler arasında ayrım yapmak için tasarlanmıştır, ancak bazı moleküller (örneğin, bazı proteinler ve biyomoleküller) en az bir boyutu 1 nm’den büyük olabilir. Birçok nanomalzeme tanımı, boyutları 1 nm’nin altında olabilen malzemeleri açıkça içerir Bu alt “nanometre” seviyesinde,malzemenin özellikleri ve nitelikleri büyük ölçüde oluşturulan nanometre malzemelerinin fiziksel doğası tarafından değil molekülün kimyası tarafından belirlenir.
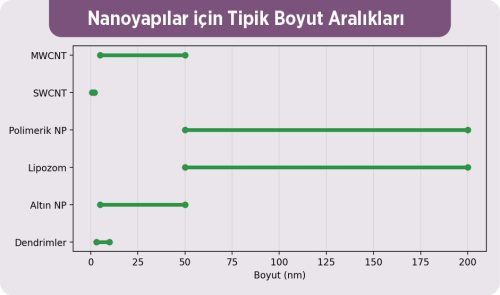
Şekil 1. Nanoyapılar için tipik boyut aralıkları (dendrim, altın NP, lipozom, polimerik NP, CNT)
2. Dağılım Eşikleri ve Kütle – Parçacık Sayısı
Boyutun bir nano nesneyi veya nanomalzemeyi nasıl tanımladığını anlamanın ek bir pratik yönü, medyan veya ortalama etrafındaki boyut dağılımıdır. Az sayıda parçacıklı madde “monodispers”tır (yani, geometrik standart sapması <2 olan).Bunun yerine, çoğu doğal olarak oluşan ve üretilen nanomalzemenin boyut dağılımları geniş ölçüde değişebilir. Şekil 2A, aynı medyan boyuta sahip iki parçacık popülasyonunun varsayımsal dağılımını göstermektedir.
Bu iki örnek için dağılım büyük ölçüde değişir, ancak parçacıkların çoğu hala nano ölçektedir (100 nm’den az). Bununla birlikte, dağılımdaki parçacıkların yalnızca bir kısmı nano ölçekteyse, bu madde bir nanomalzeme olarak kabul edilmeli midir? Şekil 2B, parçacıkların yalnızca %10’unun nano ölçekte olduğu bir parçacık boyutu dağılımını göstermektedir. Bir tanım bileşeni olarak dağılımsal bir boyut kesme noktasının dahil edilmesi, neyin nanomalzeme olarak kabul edilmesi gerektiği konusunda daha fazla netlik sağlamak için gereklidir (Bleeker vd., 2013).
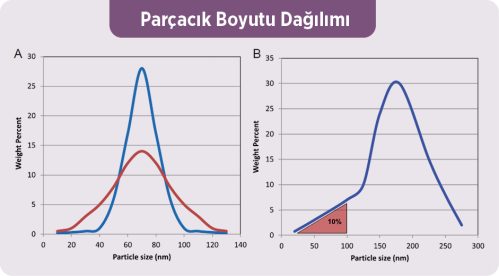
Şekil 2. Parçacık boyutu dağılımı
(A) Ortalama parçacık boyutu aynı ancak genel boyut dağılımları farklı olan iki basit parçacık popülasyonunun varsayımsal boyut dağılımı.
B) Ortalama parçacık boyutu 100 nm’den büyük olan bir maddenin, parçacık popülasyonunun bir kısmının hala 100 nm’den küçük olabileceğini vurgulayan varsayımsal bir parçacık boyutu dağılımı.
Birçok tanım, tutarsız bir şekilde de olsa, parçacık boyutu dağılımını önemli bir husus olarak içermektedir.Bazı tanımlar parçacık boyutu dağılımını ağırlık yüzdesine göre tanımlarken, diğerleri sayı dağılımına göre tanımlar. Örneğin, Avrupa Komisyonu %50’lik bir parçacık sayısı sayısı önermişken, ABD Çevre Koruma Ajansı (EPA) ağırlıkça %10’dan fazla bir sayı önermiştir. Mevcut nanopartikül metrolojisi standartları büyük ölçüde kütle ve hacim yorumlamalarına odaklanmıştır ve 100 nm’nin altına inen parçacık sayım dağılımlarını doğrulamaya yönelik sınırlı çabalar olmuştur (Brown ve ark., 2013). Bu sınırlamaya rağmen, dağılımsal bir eşik olarak kütle veya hacme odaklanmanın, daha büyük parçacıkların dağılımı çarpıtmasına ve gerçek boyut dağılımının genel olarak hafife alınmasına neden olabileceği belirtilmiştir (Bleeker ve ark., 2013). Doz ölçüm yönteminin seçimi için bir diğer husus, doz karakterizasyonunun amaçlanan kullanımıdır. Belirli bir parçacık türü ve boyutu içindeki dozun karşılaştırılması için, doz ölçüm yöntemi seçeneklerinden herhangi biri muhtemelen yeterli olacaktır. Bununla birlikte, farklı parçacık türleri ve boyut aralıkları arasında doz karşılaştırması yapılırken toksikolojik açıdan ilgili doz ölçüm yöntemi konusunda hala belirsizlik vardır.Bu durumlarda, parçacık sayısı veya yüzey alanının ilgili seçim olabileceği öne sürülmüştür (OECD, 2012).
İlginç bir şekilde, mesleki maruziyet sınırları alanında,parçacık sayısı ve kütle ölçümleri üzerine tartışmalar daha önce ele alınmış ve kütle kullanımının sağlık tehlikesini tanımlamak için daha uygun olacağı ve parçacık sayımı yaklaşımlarına göre daha basit, daha ucuz ve daha tekrarlanabilir bir yöntem sağlayacağı kabul edilmiştir (Tomb ve Haney, 1988).Ayrıca, nanomalzemeler için mesleki maruziyet sınırları (OEL’ler) üzerine yakın zamanda yapılan bir çalıştay, kütle tabanlı örnekleme ve ilgili analitik yöntemlerin, işyerinde havada bulunan partikülleri rutin olarak izlemek için en pratik yöntem olarak görüldüğünü belirtmiştir (Gordon vd., 2014).
Bu faktörlerin, nanomalzemeler için OEL gelişimini kütle tabanlı ölçüm değerlerine doğru yönlendirmesi beklenmektedir.Bir malzemenin parçacık sayısı tabanlı EC tanımını karşılayıp karşılamadığını belirlemenin analitik zorlukları yakın zamanda gözden geçirilmiştir; temel engel, standartlaştırılmış, doğrulanmış yöntemlerin eksikliğidir (JRC, 2014). JRC raporunda tanımlanan sayı tabanlı parçacık analizlerinin özel teknik zorlukları şunlardır:
- boyut dağılımını değiştirebilen numune hazırlama teknikleri;
- temsili numuneler elde etme;
- agregalar içindeki birincil parçacıkların sayılması;
- toz için dağıtım yöntemlerinin yeterliliğinin belirlenmesi;
- küresel olmayan parçacıklar için en uygun boyut ölçütünün seçilmesi (örneğin, minimum dış boyut, eşdeğer küre vb.);
- standart referans malzemelerinin uygunluğu.
Bu sorun çözülene kadar, nanomalzemelerin toksikolojik çalışmalarının, farklı ölçü birimleri arasında dönüşümlere olanak tanıyan bir şekilde parçacıkların karakterizasyonunu içermesi önerilmiştir.
Bu makul görünse de, parçacık kütlesini veya hacmini ölçmek için kullanılan laboratuvar aletlerinin, parçacık sayımı bilgilerini elde etmek için genellikle matematiksel dönüşümler kullandığını ve bu aletler için, bir yöntemin nano ölçekte kütle veya hacim dağılımını doğru bir şekilde tanımlama yeteneğindeki %1’lik bir hatanın, sayı dağılımında %50’den fazla bir hataya dönüşebileceğini (Linsinger vd., 2012;Brown vd., 2013) kabul etmek önemlidir. Ekonomik İşbirliği ve Kalkınma Örgütü’nün (OECD) görüşleri de doz sonuçlarının kütle bazlı birimlerde raporlanmaya devam etmesinin uygun ve muhtemel olduğunu ve bundan herhangi bir sapmanın verilerin uluslararası karşılıklı kabulü açısından büyük sonuçlar doğurabileceğini ve maddelerin tehlikelerinin kütle konsantrasyonuyla ilişkili olduğu sınıflandırma ve etiketlemeyi etkileyebileceğini kabul etmektedir (OECD, 2012).
3. Agregatlar ve Aglomeratlar
Üretim süreçleri, parçacıkların şekli ve parçacıkların birbirleriyle nasıl etkileşime girebileceği üzerinde önemli bir etkiye sahip olabilir.Nanomalzemeler ya “yukarıdan aşağıya” ya da “aşağıdan yukarıya” üretim yaklaşımlarıyla üretilir (Luther, 2004). Çoğu geleneksel nanomalzeme üretim süreci, daha büyük boyutlu bir malzemenin daha küçük parçacık boyutlarına öğütüldüğü veya işlendiği “yukarıdan aşağıya” yaklaşımlardır. Süreçte uygulanan enerji miktarına bağlı olarak, nihai malzemenin boyutu mikron ölçeğinden nano ölçeğe kadar değişebilir.
Bazı grafenler, grafitin mekanik olarak küçültülerek nano ölçekli boyutlara sahip grafen “tabakaları” haline getirildiği “yukarıdan aşağıya” bir yöntemle üretilen nanomalzemelere örnektir (Knieke vd., 2010). Pigmentler de yaygın olarak yukarıdan aşağıya bir yaklaşımla üretilen nanomalzemelere başka bir örnektir. Maier ve ark. (2006), akciğer sürfaktanının titanyum dioksit parçacıklarının ayrışmasını teşvik edip edemeyeceğini araştırdılar:
Akciğer sürfaktanının ana bileşeni ile titanyum dioksit arasındaki etkileşim enerjisinin, titanyum dioksit agregatlarının birincil parçacıkları arasındaki bağları ve/veya titanyum dioksit aglomeratlarının agregatları arasındaki bağları koparmak için yeterli olup olmadığını değerlendirdiler. Matematiksel modelleme kullanarak, etkileşim enerjisinin bağları koparmak için yetersiz olduğunu belirlediler. Matematiksel modeli doğrulamak için yazarlar, zaman içinde simüle edilmiş akciğer sıvısında titanyum dioksit süspansiyonlarının parçacık boyutu dağılımını ölçtüler ve parçacık boyutu dağılımında kayda değer bir değişiklik bulamadılar; bu da titanyum dioksitin simüle edilmiş akciğer sıvısında parçalanmadığını gösteriyor. Yazarlar, akciğer sürfaktanının titanyum dioksit agregatlarının veya aglomeratlarının parçalanmasını teşvik etmediği sonucuna varıyorlar.
Çeşitli maruz kalma yöntemlerini (yani trakea içi uygulama ve nano boyutlu veya mikro boyutlu parçacıklar içeren aerosollerin solunması) kullanarak, Creutzenberg ve ark. (2012), akciğerde emilimden sonra nanopartikül kümelerinin akıbetini araştırdı ve nano ölçekli parçacıkların, solunum yolu hücreleriyle etkileşime girdikten sonra daha büyük boyutlu kümeler oluşturma eğiliminde olduğunu buldu.Yazarlar, kümelerin parçalanması nedeniyle parçacık sayısındaki artışın yüksek biyolojik öneme sahip görünmediği sonucuna vardılar.
Genel olarak, mevcut bilimsel literatür göz önüne alındığında,agregat ve aglomeratların düzenleyici bir tanıma dahil edilmesi her zaman doğru olmayabilir. Özellikle, normal endüstriyel işleme veya beklenen kullanım koşulları altında daha küçük formlara ayrışmadığı gösterilen agregatlar, değerlendirme amacıyla ayrı nanomalzemeler olarak ele alınmamalıdır. Bu agregatlar, aynı malzemenin daha büyük ölçekli veya toplu formları tarafından etkili bir şekilde temsil edilen biyolojik özelliklere sahip olabilir. Bu kavramlar, nanomalzemelerin genel tanımlanması ve değerlendirilmesinde dikkate alınmalı ve çapraz okuma değerlendirmelerinde önemli olacaktır.
4. Çözünürlük
Biyolojik ve ekolojik ortamlardaki çözünürlük, nanomalzemelerin değerlendirilmesinde bir diğer önemli husustur çünkü malzemenin yalnızca moleküler kimliğe dayalı özelliklerini ve yüzey aktivitesi gibi parçacık davranışından etkilenen özelliklerini ayırt etmeye yardımcı olur. Mevcut tanımların çoğu çözünürlüğü dikkate almaz, ancak çözünürlüğün önemi Uluslararası Kozmetik Düzenlemeleri Konseyi’nin (ICCR) küresel kılavuz belgesinde (Rauscher vd., 2012) kabul edilmekte ve Avrupa Komisyonu Kozmetik Direktifi tanımına (EC, 2009) dahil edilmektedir.
Nanomalzemeler için çözünürlük açıkça tanımlanmamıştır. Hangi nanomalzemelerin çözünür olup hangilerinin olmadığını belirlemek için temel bir çözünürlük tanımı olmadan pratik bir yaklaşım, AB’nin Tüketici Güvenliği Bilimsel Komitesi’nin (SCCS) Kozmetiklerde Nanomalzemelerin Güvenlik Değerlendirmesi Rehberi’nde (SCCS, 2012) kullandığı gibi, çözünürlüğü sınıflandırmak için mevcut kılavuzları kullanmak olabilir.Bu yaklaşımı kullanarak, düşük çözünürlüğe sahip malzemeler, sulu çözünürlüğü 1 mg/L’den az olan malzemeler olarak sınıflandırılır. Bunun sonucu olarak, 1 mg/L’ye eşit veya daha yüksek çözünürlüğe sahip maddeler çözünür olarak kabul edilir.Parçacıkların iyonlara veya moleküllere hızlı ayrışması, parçacığın toksikolojisinin (ve risk değerlendirmesinin) parçacığın özelliklerine (örneğin yüzey reaktivitesi veya kristalliği) değil öncelikle moleküler kimliğine dayanması gerektiğini gösterir (SCENIHR, 2007), Biyolojik veya ekolojik sıvılarda hızla ayrışan malzemelerin özellikleri, büyük olasılıkla moleküler ve/veya iyonik formun özelliklerine bağlıdır. Bunlar moleküler formda emilir, dağıtılır ve ortadan kaldırılırken, yavaş ayrışanlar öncelikle parçacık olarak davranır. Örneğin, çinko oksit ve kadmiyum selenit (kuantum noktaları) parçacıklarının iyonlara ayrıştığı gösterilmiştir (Hardman, 2006; Xia vd., 2008; Gulson vd., 2010; Galeone vd.,2012) ve ayrışan iyonlar böylece parçacıkların biyolojik özelliklerine katkıda bulunur.
Düzenleyici amaçlar için çözünürlüğü değerlendirirken, dengedeki toplam çözünürlükten ziyade çözünme kinetiği önemli olacaktır. Çözünürlük hızı, malzemenin solunduğu zamandan temizlendiği zamana kadar olası biyolojik aktivite için mevcut olan madde miktarını ve formunu belirleyecektir. Daha az yaygın bir olgu olmakla birlikte, bazı malzemeler için nanopartiküllerin ekolojik koşullar altında çözünmüş türlerden oluşabileceği unutulmamalıdır (Slowey, 2010; Akaighe, 2011).
Çözünme ve mekanik temizleme mekanizmaları arasındaki ilişki iyi incelenmiş ve solunan partikül ve insan yapımı liflerin biyolojik etkilerini tahmin etmek için önemli olduğu gösterilmiştir (Şekil 3) (Oberdörster, 1989; Davis, 1994; Oberdörster vd., 1994; Borm vd., 2006). Bu bağlamda, mekanik temizleme mukosiliyer aktivite (esas olarak üst solunum yolu) yoluyla partikül taşınmasını, makrofajlar tarafından fagositozu ve mononükleer fagosit sistemi yoluyla göçü veya solunum epiteli yoluyla partiküllerin doğrudan translokasyonunu içerir. Örneğin, üç nano ölçekli malzeme arasındaki potansiyel biyolojik etkilerdeki farkı ele alalım: deniz tuzu (NaCl), çinko oksit (ZnO) ve titanyum dioksit (TiO2). Tuz, solunma ve mukoza ile temas üzerine neredeyse anında ayrışır. ZnO partiküllerinin ayrışma modeli daha karmaşıktır, ancak sonunda bir miktar çözünmeye yol açar (Lopes vd., 2014), oysa nano ölçekli TiO2, akciğerde haftalar süren yarı ömrüyle esasen çözünmezdir (Oberdörster vd. 1994, Bermudez vd. 2004).
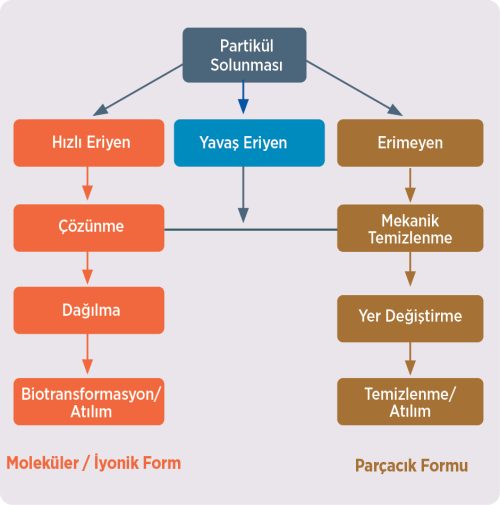
Şekil 3: Solunan partiküllerin akciğerlerden temizlenmesi.
Partiküllerin akciğerlerden temizlenmesi,çözünme veya mekanik temizleme yoluyla sağlanabilir ve bu da malzemenin genel toksisitesini etkileyebilir. Mekanik temizleme, partikül taşınmasını içerir: mukosiliyer aktivite (esas olarak üst solunum yolu), makrofajlar tarafından fagositoz vemononükleer fagosit sistemi yoluyla göç veya partiküllerin solunum epiteli yoluyla doğrudan translokasyonu.
Solunan partikül halindeki NaCl’nin temizlenmesi, hızlı çözünme ile başlar ve ardından çözünmüş iyonların emilimi ve atılımı gelir. ZnO’nun temizlenmesi başlangıçta mekanik yollarla ve çözünme yoluyla gerçekleşirken, TiO2’nin temizlenmesi biyolojik sıvılardaki sınırlı çözünürlüğü nedeniyle neredeyse tamamen mekanik yollarla gerçekleşir (Bermudez vd., 2004). Deniz tuzu maruziyetinin fiziksel formu, biyolojik etkiler açısından büyük ölçüde önemsizdir, çünkü hemen iyonik bileşenlerine ayrışır; TiO2’nin etkileri ise öncelikle fiziksel formuna bağlı olacaktır. Solunan ZnO’nun potansiyel etkileri, partikül etkilerinin (başlangıçta) ve çözünme sonucu oluşan iyonize Zn formunun etkilerinin bir karışımı olacaktır. Bu nedenle, çözünürlük ve çözünme hızının dikkate alınması, boyuta bağlı parçacık etkileri gösterme potansiyeline sahip malzemeler ile etkileri başlangıçtaki fiziksel parçacık biçimlerinden bağımsız olarak moleküler biçimden kaynaklanan malzemeler arasında ayrım yapmada önemlidir.
Çözünmeyi etkileyen faktörler arasında ortamın bileşimi,iyonik kuvvet, sıcaklık, pH ve ligandların varlığı yer alır;örneğin kanda bulunan proteinler, lipitler veya şekilli elemanlar gibi ligandlar,nanomalzemeye tercihli olarak bağlanabilir ve temizlenmenin kinetiğini değiştirebilir (Rauscher vd., 2012). Yüzey mimarisi, kaplamalar ve kümelenme durumu da çözünmeyi etkiler (Borm vd., 2006;Rauscher vd., 2012). Bu nedenle, çözünmenin kapsamını ve hızını değerlendirmek kolay değildir. Ne yazık ki, çözünme hızına göre çözünürlüğü tanımlamak için herhangi bir standart yoktur.
Kategorik ifadeler, örneğin “çözünmez” gibi ifadeler, katı parçacıklar için pek bir anlam ifade etmemektedir. Gerçekten de, solunan parçacıklar söz konusu olduğunda çözünür/çözünmez ve yavaş/hızlı temizlenmenin ne anlama geldiği konusunda çok az fikir birliği vardır.
Örneğin, amorf silikanın sıçanların akciğerlerindeki yarı ömrü yaklaşık 50 gündür, ancak esas olarak akciğer sıvısında “çözünme” yoluyla “hızlı” bir şekilde temizlendiği söylenmektedir (Fruijtier-Polloth, 2012). Bunun yerine, çözünme hızı, bir parçacığın sağlam kalıp kalmadığını veya daha fazla değerlendirmeyi yönlendirebilecek bileşenlere ayrışıp ayrışmadığını karakterize etmede daha değerli olabilir.
Biyolojik sıvılarda hızla çözünen malzemelerin biyolojik etkileri öncelikle kimyasal özellikleriyle ilgili olduğundan ve fiziksel formlarıyla ilgili olmadığından, aynı malzemelerin nano olmayan formuna verilen düzenleyici ilginin ötesinde ek bir düzenleyici ilgiyi haklı çıkaracak gibi görünmüyorlar. Muhtemelen, daha büyük ölçekli çözünebilir solunan parçacıklar, çözündükçe nano ölçekli boyut aralığından geçecek ve nano ölçekli forma özgü biyolojik etkileri gösterecektir. Bu nedenle, daha büyük parçacıklardan elde edilen toksikolojik bilgiler, nano ölçekli formun toksikolojisi için de geçerli olabilir. Sonuç olarak, çözünürlük ve çözünme, nanomalzemelerin değerlendirilmesinde dikkate alınması gereken önemli faktörlerdir.
5. Üretilen Nanomalzemeler
Nano ölçekli parçacıklar doğa için yeni bir şey değil. Dünyanın oluşumundan günümüze kadar her yerde mevcut oldular ve biz sürekli olarak nano parçacıklarla çevriliyiz. Örneğin, soluduğumuz hava, santimetre küp başına on binlerce nanopartikül içerir (Buzea vd., 2007; Hochella vd. 2008; Slezakova vd. 2013). Bu nanopartiküllerin bazıları, kömür ve petrol ürünlerinin yakılmasından kaynaklanan yanma ürünleri, aşınmadan kalan kalıntılar ve hatta fırınlama gibi insan yapımı kökenli tesadüfi parçacıklardır. Birçoğu ise hava koşulları, volkanik toz, deniz spreyi ve orman yangınları gibi doğal yanma kaynaklarından gelen doğal kökenlidir. Doğal olarak oluşan nanomalzemelerin hacmi, insan yapımı kaynaklardan üretilenlerin hacmini çok aşmaktadır (Buzea vd., 2007). Bazı çok küçük parçacıkların bileşimleri ve/veya havadaki konsantrasyonları nedeniyle sağlık sorunlarına yol açabileceği kabul edilmekle birlikte, bu malzemelere dikkat çekmek için çok küçük parçacıkların basit varlığından daha fazlasına ihtiyaç vardır.
Ticarette kullanılan nanomalzemeler için herhangi bir tanımın temel bir unsurunun yalnızca kasıtlı olarak üretilen (yani, tasarlanmış) nanomalzemeleri içermesi önerilmektedir. Bu unsurun dahil edilmesi, tesadüfen üretilen ve doğal kaynaklardan elde edilen nanomalzemelere uygunsuz bir şekilde odaklanmayı önleyerek, paydaşların belirli özelliklere sahip olmak üzere nano ölçekte kasıtlı olarak üretilen malzemelere odaklanmasını sağlayacaktır.
ISO (2010), üretilmiş ve tasarlanmış olmak üzere iki tür nanomalzeme için yararlı tanımlar sunmaktadır. Üretilmiş bir nanomalzeme, belirli özelliklere veya belirli bir bileşime (örneğin, şeffaflık) sahip olmak üzere ticari amaçlarla kasıtlı olarak üretilir.
Tasarlanmış bir nanomalzeme ise belirli bir amaç veya işlev için tasarlanmıştır (örneğin, kuantum noktaları).Her durumda, üreticilerin amacı nanomalzemenin boyutuna bağlı olarak sağladığı özelliklerden yararlanmaktır. Bu nedenle, nanomalzemenin değerlendirilmesinde kasıtlı üretimi temel bir unsur olarak ele almak uygundur. Mevcut tanımların çoğu bu önemli unsuru içermektedir (Tablo 1), ancak bunun tek tip olarak benimsenmesi gerektiği önerilmektedir.
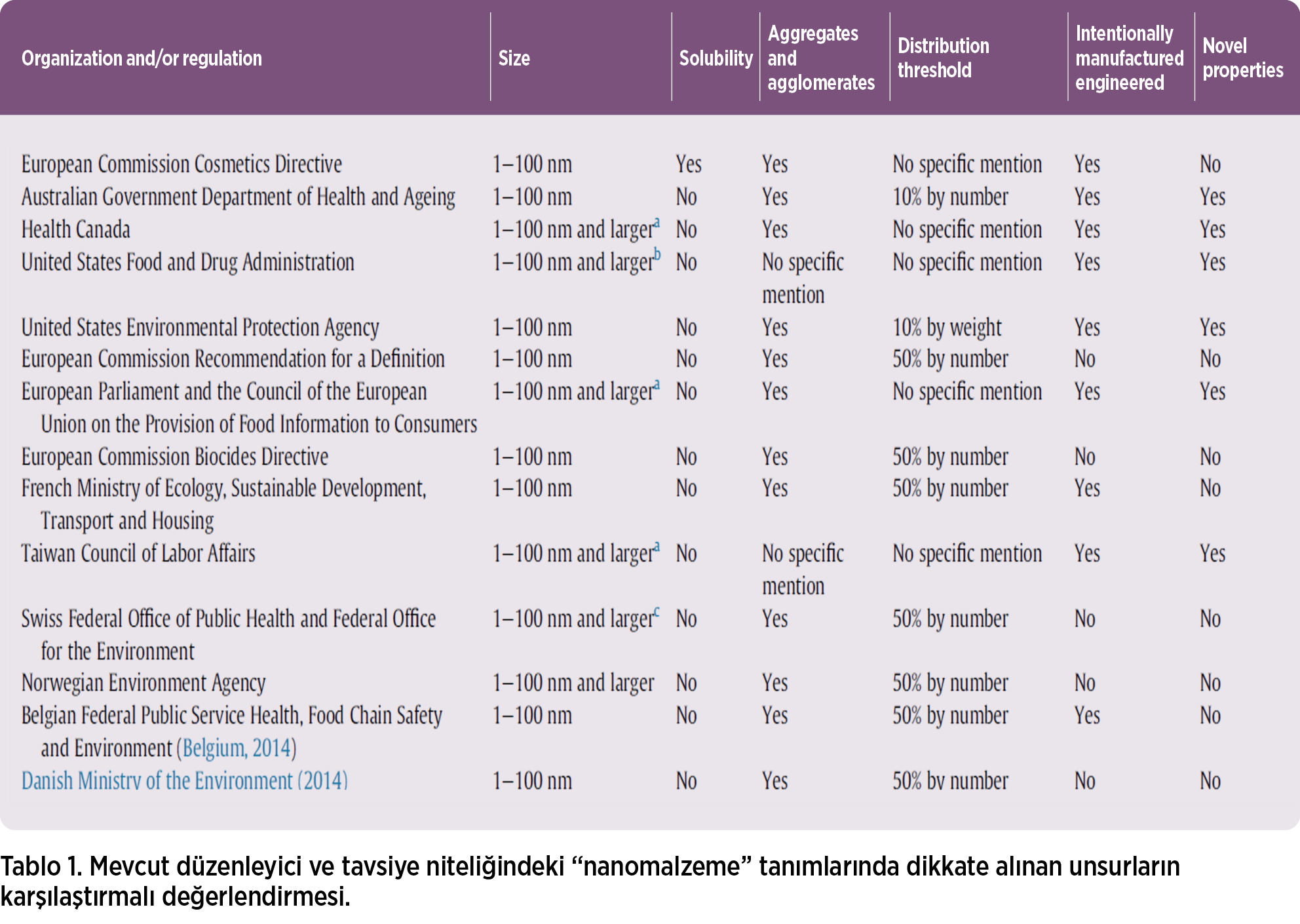
a.Kanada Sağlık Bakanlığı, Avrupa Komisyonu (gıda ve gıda ile temas eden malzemeler için) ve Tayvan Çalışma Konseyi, bir veya daha fazla nano ölçekli özellik/fenomen sergilemeleri durumunda, tüm boyutlarda nano ölçekten daha büyük malzemelerin dahil edilebileceğini belirtmiştir.
b. ABD Gıda ve İlaç İdaresi (FDA), malzemenin boyutlarından kaynaklanan özellikler veya olgular sergilemesi koşuluyla, bir mikrona kadar olan malzemeleri de kapsam içine almaktadır.
c. İsviçre tanımı, 500 nm’ye kadar birincil parçacıklara, agregatlara ve kümelenmelere sahip maddelerin yanı sıra, nano ölçekli yan dallara sahip olabilen 10 mikrona kadar solunabilir maddeleri de içerir.
Üretilmiş bir nanomalzeme, belirli özelliklere veya belirli bir bileşime (örneğin, şeffaflık) sahip olması için ticari amaçlarla kasıtlı olarak üretilir. Mühendislik ürünü bir nanomalzeme ise belirli bir amaç veya işlev için tasarlanmıştır (örneğin, kuantum noktaları). Her iki durumda da, üreticilerin amacı nanomalzemenin boyutuna bağlı olarak sağladığı özelliklerden yararlanmaktır. Bu nedenle, nanomalzemenin değerlendirilmesinde kasıtlı üretimi temel bir unsur olarak ele almak uygundur. Mevcut tanımların çoğu bu önemli unsuru içerir (Tablo 1), ancak bunun tek tip olarak benimsenmesi gerektiği belirtilmektedir.
6. Nanomalzemelerin Boyuta Bağlı Özellikleri
Nanomalzemeler tipik olarak, karşılaştırılabilir daha büyük boyutlu malzemelerde bulunmayan boyuta bağlı özelliklerden yararlanmak için geliştirilir ve kullanılır ve bu nedenle alışılmadık veya yeni olarak kabul edilirler.
Bazı nanomalzemeler için, boyuta bağlı olan ve aynı malzemenin daha büyük formlarının özelliklerine dayanarak kolayca tahmin edilemeyen özellikler vardır.
Auffan vd.’den (2009), örnekler şunlardır:
- Kalayın erime noktası, parçacık boyutu >100 nm olduğunda 232 °C’dir, ancak parçacık boyutu 6 nm olduğunda erime noktası sadece 14 °C’dir.
- Kadmiyum selenit normalde bir yarı iletkendir, ancak 5e10 nm’lik bir kuantum noktasına dönüştürüldüğünde elektronların hareketi çok daha sınırlıdır (kuantum sınırlaması), bu da daha az yoğun beyaz veya mavi ışıkla uyarıldığında dar bir dalga boyu bandında (renk) yoğun boyuta bağlı görünür ışık emisyonlarının (floresans) üretilmesine neden olur.
- Altın genellikle kimyasal olarak inert kabul edilir, bu da onu elektronik bağlantılar ve mücevherat gibi birçok uygulamada ideal bir malzeme yapar. İlginç bir şekilde, altın, parçacık boyutu nanometre ölçeğine indirildiğinde katalitik hale gelir.

Şekil 4. Boyut küçüldükçe toksisiteyi etkileyen mekanizmalar
Bunun aksine, birçok nanomalzeme, daha büyük ölçekli formlarıyla karşılaştırıldığında alışılmadık veya yeni özellikler sergilemez. Alışılmadık olmayan, boyuta bağlı bir özelliğe örnek olarak, kütleye kıyasla yüzey alanındaki değişim verilebilir. Bu özellik hem analitik hem de matematiksel olarak kolayca belirlenebilir ve belirli bir kütle için daha küçük parçacıklar daha büyük parçacıklardan daha fazla yüzey alanına sahiptir.
Bu özelliğin bir uygulaması, yüksek yüzey alanına sahip katı malzemelerin, karşılaştırılabilir miktarda düşük yüzey alanına sahip malzemeye göre daha fazla sıvıyı emebildiği emilimdedir.
Bir diğer örnek ise, katı malzemelerin plastiklerde güçlendirici madde olarak eklenebildiği ve daha küçük boyutlu malzemelerin, daha büyük parçacıklara göre belirli bir kütle için daha fazla mukavemet sağladığı takviye edici maddelerde görülmektedir. Belirtildiği gibi, bu özellik boyuta bağlıdır ancak yeni veya alışılmadık bir durum değildir (Fu ve ark., 2008).
Birçok tanım zaten “yeni” veya “benzersiz” özellikler veya “nano ölçekli olaylar” kavramını içermektedir (Tablo 1).Bununla birlikte, mevcut tanımların çoğu, tehlike değerlendirme amaçları için hangi özelliklerin yeni ve benzersiz olarak kabul edilmesi gerektiği konusunda çok az veya hiç rehberlik sağlamamaktadır ve bu özelliklerin doğru bir şekilde ölçülmesinde karşılaşılan zorlukları yeterince dikkate almamaktadır. Örneğin, yüzey reaktivitesi sıklıkla nanomalzemelerin (eko)toksikliğine önemli bir katkıda bulunan faktör olarak belirtilmektedir.
Bununla birlikte, yüzey reaktivitesini ölçmek için en uygun yöntemler konusunda bir fikir birliği yoktur ve mevcut yöntemler hatalara ve yanlış yorumlamalara eğilimli olabilir (Horst vd., 2013; Petersen vd., 2014). Bazı tanımlar, bu alışılmadık özelliklerin 100 nm’den büyük malzemelere genişletilmesini içermektedir ve bu durumlarda tanım kılavuzunun daha büyük malzemelerin dahil edilmesinin temelini açıkça belirtmesi önerilir.
Genel olarak, nanomalzemelerin tanımlanması ve değerlendirilmesinde tutarlılık ve şeffaflığı sağlamak için bu alanda ek tartışma ve açıklık kritik önem taşımaktadır. Yukarıda tartışılan unsurlar –parçacık boyutu, dağılım eşiği, kasıtlı üretim, kümelenme/kümelenmenin çözülmesi ve kümelenme/parçalanmanın çözülmesi durumu, çözünürlük/çözünme hızı ve çökelme/yeniden oluşma ve ilgili boyuta bağlı özellikler– nanomalzeme tanımlarını tartışırken veya değerlendirme çerçeveleri oluştururken dikkate alınması gereken önemli bileşenleri temsil etmektedir. Sadece parçacık boyutuna dayalı tamamen teknik nanomalzeme tanımları, örneğin ISO’nun tanımı (ISO, 2008), güvenlik değerlendirmesi açısından yararlı değildir çünkü parçacık formunda bulunabilecek hemen hemen her maddeyi içerebilirler. Nanomalzeme değerlendirme çerçeveleri, insan sağlığını ve çevreyi koruma amacıyla ek değerlendirmeyi hak edebilecek nanomalzemelere odaklanmaya yardımcı olmak için oluşturulmalı;aynı zamanda kapsam açısından uygun netliğe sahip olmalı ve uygulanması pratik olmalıdır.
Nanotoksikoloji-Geçmişten Geleceğe
Nanotoksikoloji terimi, son yirmi yıldan itibaren ilgi görmeye başlamıştır ( Singh, A.V., 2019, Doktorovova, S.,2014, Doktorovova, S.,2016).
İki önemli faktör, bu bilim dalında hızlı bir ilerlemeye yol açmıştır (Jeevanandam, J.; 2018). Birincisi, “çeşitli nanomalzemelerin büyük ölçekli üretimi ve şaşırtıcı fiziksel ve kimyasal özelliklere sahip yeni tip nanomalzemelerin geliştirilmesinde kayda değer ilerleme”. İkincisi, sürekli olarak geliştirilen NM’lere dayalı birçok çalışma, Fizik, Kimya ve Biyomühendislik alanlarında araştırmaları teşvik ederek Nanobilim ve uygulamalarında yeni disiplinlerarası ilerlemelere yol açtı. Örneğin, NM’lerin biyolojik uygulamalarında büyük ilerleme kaydedildi (Shvedova, A.,2016).
Nanotıp ve nanotoksikoloji, her ikisi de aynı mekanizmaları ve aynı metabolik yolları keşfedebildiği için yakından bağlantılıdır (Oberdörster, G.2010). Yeni NM’lerin spesifik toksisite gösterebileceği göz önünde bulundurulduğunda, zaman zaman biriken verileri özetlemek ve yeniden değerlendirmek, böylece güvenliği sağlamak gereklidir (Gaur, N., 2020). Mevcut nanotoksikoloji çalışmalarının gelişimi, özellikle biyolojik alanda hız kazanmıştır. Örneğin, bitkiler ve diğer botanik ürünler aracılığıyla insektisit nanopartiküllerin biyosentezi sürekli olarak geliştirilmektedir (Severino, P.,2017, Diniz, F.R.,2020). Son 20 yılda nanotoksikoloji, toksikoloji ve NM’lerin arayüzünde bir alt disiplin haline gelmiştir (Shvedova, A.,2016). Son derece küçük boyutları ve hacim oranına göre geniş yüzey alanı nedeniyle, NM’ler, hücreler ve dokularla öngörülemeyen etkileşimlere olanak sağlayabilecek daha büyük muadillerine kıyasla farklı özelliklere sahiptir. Nanotoksikoloji, NM’ler ile farklı biyolojik sistemler (hücreler,dokular ve canlı organizmalar) arasındaki olası toksik etkileşimleri vurgulamaya eğilimlidir. Yıllarca süren araştırmalar, NM’lerin çevre ve canlı organizmaların hücreleriyle etkileşimlerinin son derece karmaşık olduğunu göstermiştir (Souto, E.B.,2020, Doktorovova, S.,2014). Bununla birlikte, NM’lerin özelliklerinin (hem fizikokimyasal hem de morfolojik) bu etkileşimleri nasıl etkileyebileceği henüz ortaya çıkarılmamıştır (Giner-Casares, J.J.,2016, Marambio-Jones, C.,2010, Lee, J.,2010).
Nanomalzemelerin morfolojik ve fizikoşimik özellikleri, biyolojik hücrelerle etkileşim üzerinde büyük bir etkiye sahiptir ve toksisitelerini etkileyebilir. Nanotoksikoloji, özellikle malzemelerin boyutu nanomalzemelerin toksisitesinde önemli bir rol oynadığından, nanomalzemelerin toksik etkilerinin analizinden sorumludur (Nel, A.E.;2009). Nanotoksikoloji kavramı, boyut, yüzey alanı, morfoloji, bileşim, yüzey kimyası, kümelenme/agregasyon olayları vb. gibi farklı parametrelere dayanmaktadır. Aslında, bu parametrelerin tümü, nanopartiküllerin dozunun belirlenmesinde ve dolayısıyla toksisitelerinin kesin değerlendirilmesinde kritik bir etkiye sahiptir. Ancak, toksik NM’lerin maksimum maruz kalma değerlerinin belirlenmesi, in vitro ve in vivo testler olmadan imkansızdır.
Nanoparçacıkların Etkisi: İn Vitro ve İn Vivo Çalışmalar
Titanyum dioksit ve gümüş nanopartiküller, sağlık, çevre ve endüstriler gibi çeşitli alanlardaki çok yönlülükleri ve işlevsellikleri nedeniyle en yaygın kullanılan nanomalzemelerdir ve ekonomiye olumlu bir etki yapmaktadırlar.
Titanium Dioxide Nanopartiküller
Titanyum dioksit (TiO2), çeşitli malzemelerde (örneğin, kağıt, plastik, seramik, kauçuk, yazıcı mürekkebi, zemin kaplamaları, katalizörler, kumaşlar ve tekstil ürünleri, kozmetik ürünler, gıda boyaları, ilaçlar, boyalar, kaplamalar ve elektronik bileşenler) kullanılmaktadır. TiO2 bazlı NM’lerin farklı türleri dört farklı kristal yapı ile ayırt edilebilir: rutil, anatas, brookit veya titanyum dioksit, rutil ve anatas ürün tüketiminde en sık kullanılanlardır.
Gümüş Nanoparçacıklar
Gümüş nanoparçacıklar (AgNPs) şu anda en çok incelenen nanomalzemelerden biridir (Ottoni, C.; 2020, Barbosa, G.P. 2016, Teixeira,M.C. 2020). Bu nanoparçacıklar, karakteristik özellikleri (örneğin, kimyasal kararlılık, şekillendirilebilirlik, esneklik, yüksek elektriksel ve termal iletkenlik, katalitik aktivite, nispeten düşük üretim maliyeti ve bakteri, virüs, mantar ve protozoalara karşı antimikrobiyal etki) nedeniyle endüstriyel ve ticari açıdan en çok kullanılanlardır.
Bu nedenle, AgNPs çeşitli uygulamalarda ve ticari ürünlerde yaygın olarak kullanılmaktadır; örneğin antibakteriyel, antifungal, antiviral, antiinflamatuar, antitümör, rejeneratif, biyosensör ve katalizör ajanları gibi. Bunlara ek olarak, gıda, tekstil, parfümeri, ilaç, tarım, hijyen, temizlik ürünleri, boyalar, elektronik endüstrileri ve diğer sektörlerdeki ürünlerde de bulunmaktadırlar ve bu da insan ve çevre maruziyetine yol açmaktadır (Marin, S.;2015). Ayrıca AgNP’lerin tıpta tıbbi cihazları kaplamak, nanogeller hazırlamak veya cilt lezyonları için formülasyonlar üretmek gibi geniş uygulama alanları vardır (Wei, L. 2015).
Nanotoksikoloji, nanomalzemelerin biyolojik sistemlerle etkileşimini ve olası zararlı etkilerini incelemektedir. Nanomalzemelerin (NM’ler) toksikolojik profillerini etkileyebilecek farklı özellikleri vardır. Bu nedenle, NM’lerin güvenli tasarımı ve uygulamasına olanak sağlamak için resmi nanotoksiklik kılavuzları oluşturulmuştur (Singh, A.V.; 2019, Doktorovova, S.;2014)
Bunlar şunları içerir: (1) parçacık boyutu, çünkü NM’lerin daha küçük boyutlarıyla toksisite ve hücreler tarafından alım artacaktır; (2) parçacık yükü, çünkü pozitif yüklü NM’ler, negatif yüklü biyolojik yüzeylerle artan etkileşimler nedeniyle daha yüksek toksisiteye sahiptir (Doktorovova, S.,2015). (3) iyonik çözünme, çünkü daha yüksek iyonik çözünme daha yüksek toksisiteye yol açar ve (4) şekil, çünkü anizotropik veya çubuk şeklindeki NM’ler daha az etkilidir ve hedef hücreleri yok edebilecek yakın kızılötesinde önemli hasara neden olabilir ( Doktorovova, S.;2016, Albanese, A.;2012)
Nanotoksikologların temel endişesi, NM’lerin neden olduğu risk faktörlerini belirlerken insan sağlığının korunmasıdır. Bu belirleme büyük bir zorluktur, çünkü insanlar kontrolsüz, saflaştırılmamış ve karmaşık süreçlerle üretilen bileşiklere entegre edilmiş NM’lere kolayca maruz kalabilirler. (Johnston, H.,2013). Bu nedenle, öngörülen nanomalzemelerin potansiyel riskini değerlendirirken dikkatli olunmalı (Warheit, D.B., 2018) ve aşağıdaki ana hatlar dikkate alınmalıdır:
- nanotoksikoloji araştırması için NM’leri seçmekve maruz kalma koşulları (fiziksel, kimyasal ve biyotik) ve maruz kalma süreleri olan ortamlar oluşturmak;
- maruz kalma araçlarının tüm özelliklerini tanımlamak ve ayrıntılı çapraz karşılaştırmalara olanak tanıyan meta verileri sunmak;
- ölçekli konsantrasyonlarda tasarlanmış NM formlarını (homojen bir değerlendirme sağlamak için risk değerlendirme süreciyle karakterize edilmiş) seçmek;
- tasarlanmış NM’lerin karakterizasyonu için çeşitli uç noktaları incelemek ve seçmek (örneğin, fizikokimyasal özellikler ve toksisite karakterizasyonu);
- tasarlanmış NM’lerin yükünü ve bölümlenmesini nicelleştirmek, böylece biyolojik yanıtta etkili dozların karşılaştırılmasını sağlamak;
- deneysel kontrol tedavilerini takip etmek; ve ilgili bilgileri elde etmek için uygun hızlı tarama biçiminde yaklaşmak.
Unutulmamalıdır ki çalışmaların çoğu belirli maruz kalma koşulları altında yürütülmekte ve oldukça anlamlı sonuçlar sunmamaktadır. Karakterizasyon ve tanımlamanın yanı sıra, NM’lerin diğer bazı risk faktörleri şunlardır: (1) büyük miktarlarda tasarlanmış NM’yi serbest bırakan ortak süreçlerin bulunması (ya büyük ölçekli nano endüstrisinin olmaması ya da NM’lerin diğer bileşiklerle entegrasyonu nedeniyle); (2) serbest bırakma işlemi sırasında NP’lerin diğer (toksik olmayan) bileşiklerle agregasyonu; (3) in vitro testler sırasında NM’lerin risk tanımlaması; (4) NM’lerin biyolojik sistemlerle etkileşiminin karmaşıklığının anlaşılması; (5) NM’ler arasındaki en küçük farkın, NM’lerin biyolojik sistemlerle etkileşiminde in vivo olarak büyük değişikliklere yol açabileceği gerçeği; (6) NM’lerin büyük değişkenliği ve dinamik dönüşümü ile ilişkili biyolojik sistemlerin karmaşıklığı; (7) deneylerin tekrarlanabilirliğini engelleyen aletlerin, uyumlu protokollerin ve teorik anlayışın eksikliği; ve (8) biyobelirteçlerle standartlaştırılmış deneylerin, gösterici fonksiyonel analizlerin, dozlamanın ve istatistiklerin eksikliği (Borm, P.J.,2006).
Sağlık Etkileri (Solunum, Sistemik ve Nörolojik)
İnhale edilen nanoparçacıklar alveoler bölgede birikerek akut inflamasyonu tetikler; alveoler makrofaj aktivasyonu, sitokin salınımı ve nötrofilik infiltrasyon tipiktir. Çoklu malzeme tiplerini kapsayan geriye dönük analizler, akut akciğer inflamasyonu için partikül yüzey alanının kütle/sayı metriklerine kıyasla daha güçlü bir doz–yanıt ilişkisi sunduğunu göstermiştir. Amorf silika NP için sistematik derlemelerde daha küçük boyut = daha yüksek sitotoksisite bulgusu baskındır; metal/metal oksit NP’lerde ROS üretimi ve oksidatif stres aracılı mekanizmalar membran/DNA/protein hasarı ve inflamasyon zincirini destekler.
CNT/CNF maruziyetinde hayvan modellerinde inflamasyon ve fibrozis güçlüdür; MWCNT‑7 tipi IARC Grup 2B (muhtemel kanserojen) olarak sınıflandırılmıştır. Biyopersistans malzeme/doza bağlıdır; nikel oksit NP’lerde akciğer yarı‑zamanlarının aylar ölçeğinde olabileceği rapor edilmiştir. NP’ler dolaşıma geçerek karaciğer, dalak, böbrek ve beyin gibi organlara dağılabilir; nörolojik erişim için burun–beyin (olfaktor/trigeminal) yollar deneysel olarak gösterilmiş olsa da insanda klinik önemi konusunda belirsizlik sürmektedir.
Uluslararası Değerlendirmeler ve Kılavuzlar
WHO (2017) işyerlerinde üretilmiş nanomalzemeler için ihtiyat yaklaşımı ve kontrol hiyerarşisini önermekte; gruplama (lif/granüler/özel toksisite) ve eğitim/katılım vurgulanmaktadır. ISO/TS 12901‑1:2024, ENM’lere özgü risk yönetimi prensiplerini güncellemiştir. NIOSH, TiO₂ (ultrafin 0,3 mg/m³; fine 2,4 mg/m³), CNT/CNF ve gümüş için maruziyet örnekleme ve değerlendirme rehberleri yayımlamıştır. OECD, işyeri ve tüketici maruziyet araçları için performans ve duyarlılık değerlendirmelerini derlemiştir.
Maruz Kalım Değerlendirmesi: Çok Metrikli Yaklaşım ve Belirsizlikler
Tek bir metrik bütün ENM’ler için yeterli değildir. Pratikte parçacık sayısı (PNC; CPC/SMPS), kütle (gravimetri/elemental), yüzey alanı ve morfoloji/kimya (TEM/SEM, ICP‑MS) birlikte kullanılmalıdır. Cihazların dinamik üst sınırları, arka plan UFP ile karışma, kişisel örneklemedeki lojistik kısıtlar ve metot standardizasyonu önemli belirsizlik kaynaklarıdır. Proses‑spesifik örnekleme ile mühendislik kontrollerinin etkinliği doğrulanabilir. İnsan uzun dönem verisi sınırlıdır; işçi kohortlarında prospektif izlem ve çoklu metrikli doz–yanıt analizlerine ihtiyaç vardır. Saha ölçümlerinde arka plan partikülleri kaynak ayrımını zorlaştırı. Düzenleyici uyum için REACH nanoform kayıtları ve WHO/ISO rehberleri kritik önemdedir.
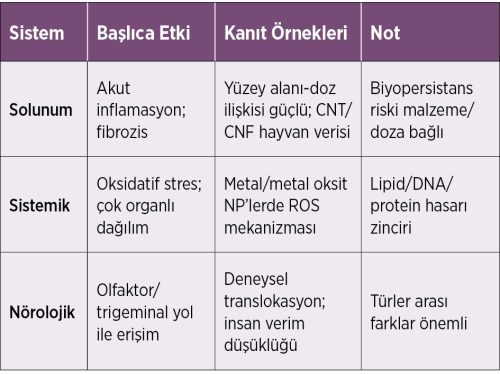
Tablo 2. Sağlık Etkileri – Sistem Ve Kanıt Özeti
Nörolojik Translokasyon: Mekanizmalar, Kanıtlar ve Belirsizlikler
Nanoparçacıkların merkezi sinir sistemine erişimi üç ana yolla gerçekleşebilir: (i) burun mukozasından olfaktor sinir (CN I) aracılığıyla koku soğanına doğrudan taşınma, (ii) trigeminal sinir (CN V) üzerinden beyin sapına erişim, (iii) sistemik dolaşıma geçen NP’lerin kan‑beyin bariyerini aşması. Hayvan modellerinde TiO₂, karbon bazlı NP ve metal oksit NP’lerin burun–beyin yoluyla hipokampus ve serebral kortekste saptandığı rapor edilmiştir. Postmortem insan bulguları, olfaktor bölgede ultrafine partikül varlığını göstermiştir; ancak işyeri maruziyetiyle doğrudan ilişki kurmak zordur. Klinik düzeyde nöroinflamasyon ve oksidatif stres belirteçleri deneysel olarak güçlüdür; insanda semptomatik korelasyon (koku alma bozukluğu, bilişsel etkiler) için kanıt sınırlıdır. Türler arası anatomik farklar translokasyon verimini etkiler; rodentlerde olfaktor epitel yüzeyi insana göre daha geniştir, bu nedenle insanda verim genellikle <%5’tir. Gerçek maruziyet koşullarında düşük doz–uzun süreli etkiler hâlâ belirsizdir. Araştırma öncelikleri: prospektif insan kohortları, nöroinflamasyon biyobelirteçleri ve görüntüleme korelasyonları olarak belirtilmektedir.
Sistemik etkiler: Dolaşımsal ve kardiyovasküler sistem üzerinde oksidatif stres ve inflamasyon aracılı etkiler olasıdır; uzun dönem insanlar için kanıt sınırlı olmakla birlikte ihtiyatlı yaklaşım önerilir.
Nazal‑beyin: Olfaktör ve trigeminal yollar üzerinden düşük verimli de olsa nanoparçacık geçişi deneysel olarak gösterilmiştir; insanlar için tür farklılıkları ve nazal anatomi farkı nedeniyle ekstrapolasyon sınırlıdır. İşyerinde bu, burunla yakın temas ve aerosol oluşumu olan süreçlerde ek korumayı gerektirir.
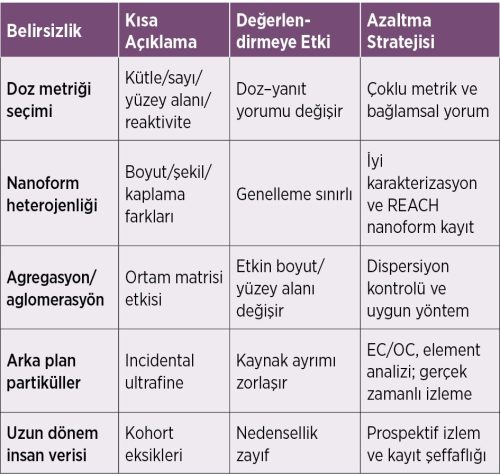
Tablo 3. Belirsizlik Kaynakları ve Değerlendirmeye Etkisi
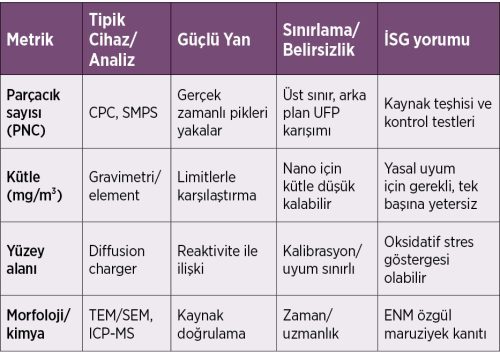
Tablo 4. İşyerinde nanoparçacık ölçüm metrikleri ve belirsizlik kaynakları
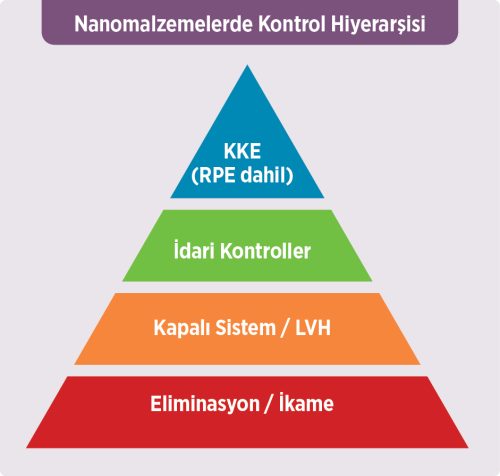
Şekil 4. Nanomalzemelerde kontrol hiyerarşisi (eliminasyon→mühendislik→idar→KKE)
Risk Yönetimi: WHO/ISO/NIOSH ile Uyumlu Uygulamalar
Kontrol hiyerarşisi:
(eliminasyon/ikame → kapalı sistem/yerel havalandırma → idari kontroller → KKE) temelinde ENM’lere özgü önlemler planlanmalıdır.
KOBİ ölçeğinde uygulanabilir basamaklı yaklaşım WHO ve ISO/TS 12901‑1:2024’te vurgulanmaktadır.
NIOSH 2022 raporu CNT/CNF, TiO₂ ve gümüş için örneklemeyi ayrıntılandırır.
Türkiye’de Mevzuat ve Uygulama: KKDİK, SEA (CLP‑TR) ve SDS
- KKDİK (23.06.2017) AB REACH ile uyumlu çerçevedir; kademeli kayıt tarihleri şöyledir: ≥1000 t/y ve CMR 1A/1B ≥1 t/y ile H400/H410 ≥100 t/y için 31.12.2026;
- 100–1000 t/y için 31.12.2028;
- 1–100 t/y için 31.12.2030.
SEA (CLP‑TR) sınıflandırma ve etiketlemeyi düzenler. 31.12.2023 itibarıyla SDS’lerin KKDİK Ek‑2 formatında, Türkçe ve Kimyasal Değerlendirme Uzmanı onaylı olması zorunludur. R7‑1 nanomalzeme rehberi Türkçe uyarlanmıştır. İşyeri hekimleri için pratik olarak: kullanılan maddelerin SDS’lerinde “nanoform” ifadesi ve karakterizasyonunun yer aldığını, maruz kalma senaryolarının prosesle uyumlu olduğunu doğrulamak kritik önem taşır.
İşyeri Hekimi Bakış Açısı Nasıl Olmalıdır?
- Nanomalzemelerin biyolojik etkilerini anlamak, risk iletişimi ve çalışan farkındalığını artırmak için eğitim planları oluşturun.
- SDS belgelerinde nanoform bilgilerini kontrol edin, belirsizlikler konusunda çalışanlara bilgi verin.
- WHO ve ISO rehberlerini uygulayın, kontrol hiyerarşisini işyeri prosedürlerine entegre edin.
- Çok metrikli ölçüm planlarını iş hijyeni ekibiyle koordine edin, spirometri ve biyobelirteç takibi yapın.
- Eliminasyon ve mühendislik kontrollerinin etkinliğini izleyin, KKE kullanımını denetleyin.
- KKDİK ve SEA uyumunu doğrulayın, SDS güncellemelerini takip edin, çalışan eğitimlerini düzenleyin.
- Belirsizlikleri yönetmek için ihtiyatlı yaklaşım benimseyin, sağlık gözetimi ve risk iletişimini sürekli iyileştirin.
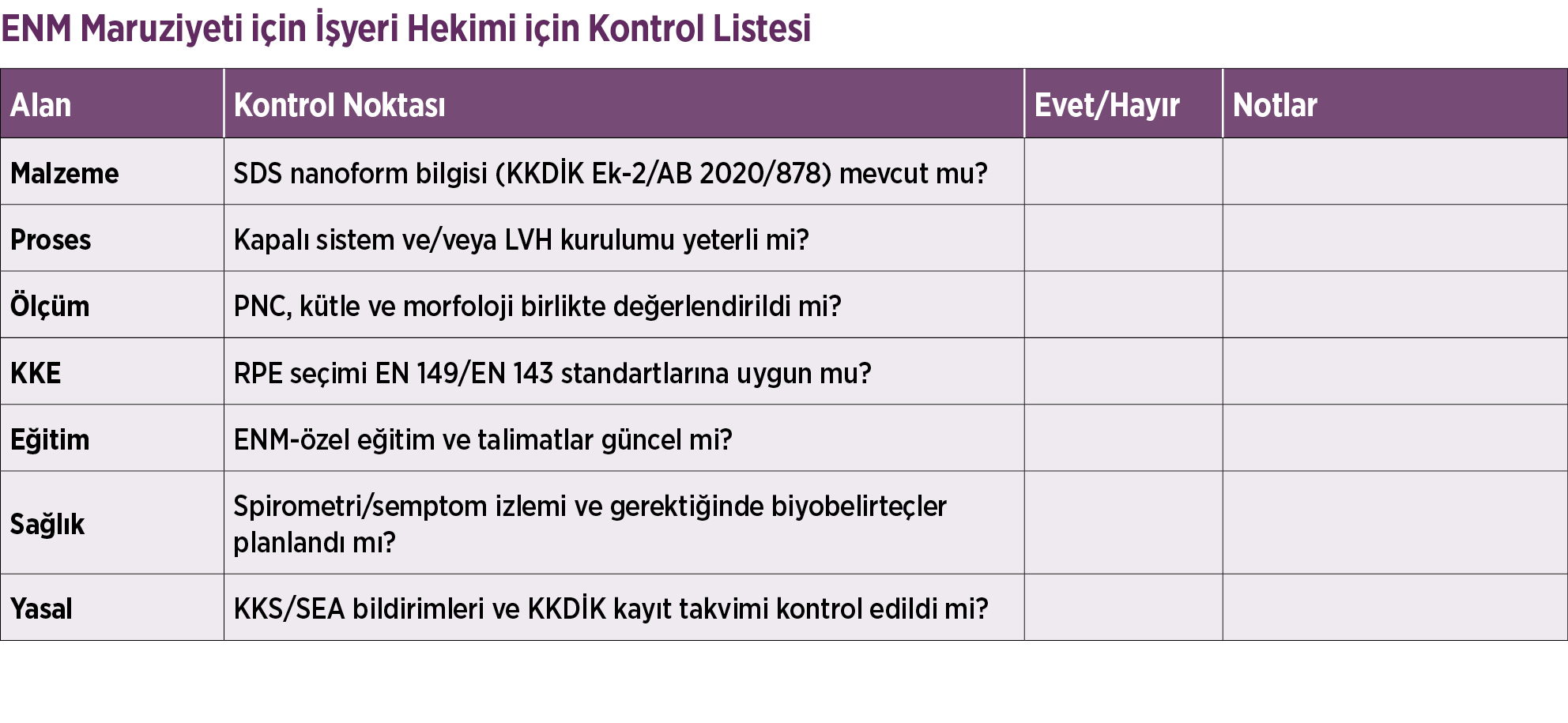
İşyeri Pratiği İçin Hızlı Kontrol Listesi
- Ölçüm planı: Kütle (mg/m³) + sayı (1/cm³, CPC/SMPS) + LDSA (m²/m³) + EC/OC (CNT/CNF) + gerektiğinde TEM/SEM+EDS.
- Kontroller: Eliminasyon/ikame → mühendislik (kapalı sistem, LEV, HEPA) → idari (SOP, erişim kısıtı, eğitim) → KKD (P100/N99; MPPS dikkati).
- Sağlık gözetimi: Semptom/fizik muayene, spirometri, endikasyon varsa görüntüleme; FeNO vb. göstergeleri maruziyet kayıtlarıyla korelasyonda kullanın.
- Düzenleyici uyum: REACH nanoform kayıtları; SDS güncellemeleri; tedarikçi karakterizasyon dosyaları; set of similar nanoforms için bilimsel gerekçe.
Proses aerosol oluşturuyor mu?
Hayır: Periyodik alan izleme.
Evet: Gerçek zamanlı sayı/LDSA + kişisel filtre; CNT/CNF: NIOSH 5040 (EC); metal/oksit: ICP‑MS/OES ve TEM/SEM+EDS; sonuçlara göre mühendislik kontrollerini doğrula ve iyileştir.
Nano Maruziyet Yönetimi Akışı (OSHA/ILO)
[Tehlike Tanımlama] → [Risk Değerlendirme] → [Ölçüm Planı] → [Veri Analizi] → [Kontrol Tasarımı] → [Uygulama ve Eğitim] → [Sağlık Gözetimi] → [Gözden Geçirme] → (Sürekli İyileştirme)
SONUÇ
Boyut bağımlı toksisite ve ölçüm belirsizlikleri, nanomalzemelerle çalışan işyerlerinde risk yönetimini zorlaştırmaktadır. Çok metrikli ölçüm stratejisi, mühendislik kontrolleri ve Türkiye’de KKDİK‑SEA gerekliliklerine uygun SDS/etiket yönetimi güvenli çalışma için temel dayanaklardır.
Nanotoksikolojide sağlık etkileri ise çok sistemli olup, akciğer inflamasyonu/fibrozisi başta olmak üzere sistemik ve nörolojik yolları içermektedir. Maruz kalım değerlendirmesindeki belirsizlikler—özellikle doz metrikleri, nanoform heterojenliği ve insan uzun dönem verisi sınırlılığı—çoklu metrik ölçüm, mühendislik kontrolleri ve risk odaklı sağlık gözetimi ile yönetilebilir. Bununla birlikte,endüstriyel ölçekli süreçler, biyosistemlerle etkileşimlerin anlaşılması (insanlara ve çevreye etki) ve düzenleme sorunları gibi birçok önemli zorluğun hala üstesinden gelinmesi gerekmektedir. Nanomalzemelerin kullanımının toksikolojik risklerinin taranması, insan sağlığı ve çevre üzerinde istenmeyen etkilere neden olma potansiyel riskinin haritalandırılması gerekmektedir. Son bilimsel raporlara dayanarak, yaygın olarak kullanılan yöntemlerin, maddelerin tehlikelerini minimumda tutarken daha etkili nanomalzemeler tasarlamaya yardımcı olduğu gözlemlenmiştir. Nanotıp alanında nanotoksikolojinin önemi, özellikle ilaç nanotaşıyıcılarının toksisitesini önlemek açısından büyük önem taşımaktadır.
 Kaynaklar:
Kaynaklar:
-
WHO (2017). Guidelines on protecting workers from potential risks of manufactured nanomaterials.
-
ISO/TS 12901‑1:2024. Nanotechnologies — Occupational risk management applied to ENMs.
-
NIOSH (2022). Occupational exposure sampling for engineered nanomaterials (TiO₂, CNT/CNF, Ag).
-
OECD (2021). Evaluation of tools and models for nanomaterial exposure (ENV/CBC/MONO…).
-
EU (2022/C 229/01). Commission Recommendation on the definition of nanomaterial.
-
NIST/DOE. The Scale of Things; Science Learning Hub; CLRN/NanoSense.
-
Doktorovova, S.; Souto, E.B.; Silva, A.M. Nanotoxicology applied to solid lipid nanoparticles and nanostructured lipid carriers – a systematic review of in vitro data. Eur. J. Pharm. Biopharm. 2014, 87, 1–18. [CrossRef] [PubMed] Lee, S.H.; Jun, B.-H. Silver Nanoparticles: Synthesis and application for nanomedicine. Int. J. Mol. Sci. 2019, 20, 865. [CrossRef]
-
Bajaj, S.; Haverty, M.G.; Arróyave, R.; Shankar, S. Phase stability in nanoscale material systems: Extension from bulk phase diagrams. Nanoscale 2015, 7, 9868–9877. [CrossRef]
-
Mourdikoudis, S.; Pallares, R.M.; Thanh, N.T. Characterization techniques for nanoparticles: Comparison and complementarity upon studying nanoparticle properties. Nanoscale 2018, 10, 12871–12934. [CrossRef]
-
Lin, M.; Fu, Z.Y.; Tan, H.R.; Tan, J.P.Y.; Ng, S.C.; Teo, E. Hydrothermal synthesis of CeO2 nanocrystals: Ostwald ripening or oriented attachment? Cryst. Growth Des. 2012, 12, 3296–3303. [CrossRef]
-
Doktorovova, S.; Kovacevic, A.B.; Garcia, M.L.; Souto, E.B. Preclinical safety of solid lipid nanoparticles and nanostructured lipid carriers: Current evidence from in vitro and in vivo evaluation. Eur. J. Pharm. Biopharm 2016, 108, 235–252. [CrossRef]
-
Doktorovova, S.; Silva, A.M.; Gaivao, I.; Souto, E.B.; Teixeira, J.P.; Martins-Lopes, P. Comet assay reveals no genotoxicity risk of cationic solid lipid nanoparticles. J. Appl. Toxicol. 2014, 34, 395–403. [CrossRef] [PubMed]
-
Albanese, A.; Tang, P.S.; Chan,W.C. The e_ect of nanoparticle size, shape, and surface chemistry on biological systems. Annu. Rev. Biomed. Eng. 2012, 14, 1–16. [CrossRef] [PubMed]
-
Johnston, H.; Pojana, G.; Zuin, S.; Jacobsen, N.R.; Møller, P.; Loft, S.; Semmler-Behnke, M.; McGuiness, C.; Balharry, D.; Marcomini, A. Engineered nanomaterial risk. Lessons learnt from completed nanotoxicology studies: Potential solutions to current and future challenges. Crit. Rev. Toxicol. 2013, 43, 1–20. [CrossRef]
-
Warheit, D.B. Hazard and risk assessment strategies for nanoparticle exposures: How far have we come in the past 10 years? F1000Research 2018, 7. [CrossRef] [PubMed]
-
Borm, P.J.; Robbins, D.; Haubold, S.; Kuhlbusch, T.; Fissan, H.; Donaldson, K.; Schins, R.; Stone, V.; Kreyling, W.; Lademann, J. The potential risks of nanomaterials: A review carried out for ECETOC. Part. Fibre Toxicol. 2006, 3, 11. [CrossRef]
-
Hjorth, R.; van Hove, L.; Wickson, F. What can nanosafety learn from drug development? The feasibility of “safety by design”. Nanotoxicology 2017, 11, 305–312. [CrossRef]
-
Kraegeloh, A.; Suarez-Merino, B.; Sluijters, T.; Micheletti, C. Implementation of safe-by-design for nanomaterial development and safe innovation: Why we need a comprehensive approach. Nanomaterials 2018, 8, 239. [CrossRef]
-
Gottardo, S.; Alessandrelli, M.; Amenta, V.; Atluri, R.; Barberio, G.; Bekker, C.; Bergonzo, P.; Bleeker, E.; Booth, A.; Borges, T. NANoREG Framework for the Safety Assessment of Nanomaterials; European Commission Joint Research Centre: Ispra, Italy, 2017.
-
Mohs, R.C.; Greig, N.H. Drug discovery and development: Role of basic biological research. Alzheimer’s Dement. Transl. Res. Clin. Interv. 2017, 3, 651–657.
-
Ahuja, V.; Sharma, S. Drug safety testing paradigm, current progress and future challenges: An overview. J. Appl. Toxicol. 2014, 34, 576–594. [CrossRef]
-
Merlot, C. Computational toxicology—A tool for early safety evaluation. Drug Discov. Today 2010, 15, 16–22. [CrossRef]
-
Siramshetty, V.B.; Nickel, J.; Omieczynski, C.; Gohlke, B.-O.; Drwal, M.N.; Preissner, R. WITHDRAWN—A resource for withdrawn and discontinued drugs. Nucleic Acids Res. 2016, 44, D1080–D1086. [CrossRef] [PubMed]
-
Jeevanandam, J.; Barhoum, A.; Chan, Y.S.; Dufresne, A.; Danquah, M.K. Review on nanoparticles and nanostructured materials: History, sources, toxicity and regulations. Beilstein J. Nanotechnol. 2018, 9, 1050–1074. [CrossRef] [PubMed]
-
Shvedova, A.; Pietroiusti, A.; Kagan, V. Nanotoxicology ten years later: Lights and shadows. Toxicol. Appl. Pharmacol. 2016, 299, 1–2. [CrossRef] [PubMed]
-
Oberdörster, G. Safety assessment for nanotechnology and nanomedicine: Concepts of nanotoxicology. J. Intern. Med. 2010, 267, 89–105. [CrossRef] [PubMed]
-
Gaur, N.; Sharma, N.; Dahiya, A.; Yadav, P.; Ojha, H.; Goyal, R.K.; Sharma, R.K. Toxicity and Regulatory Concerns for Nanoformulations in Medicine. ELSI Handb. Nanotechnol. 2020, 5, 333–357. [CrossRef]
-
de Souza, A.L.; Andreani, T.; de Oliveira, R.N.; Kiill, C.P.; dos Santos, F.K.; Allegretti, S.M.; Chaud, M.V.; Souto, E.B.; Silva, A.M.; Gremiao, M.P. In vitro evaluation of permeation, toxicity and e_ect of praziquantel-loaded solid lipid nanoparticles against Schistosoma mansoni as a strategy to improve e_cacy of the schistosomiasis treatment. Int. J. Pharm. 2014, 463, 31–37. [CrossRef]
-
Diniz, F.R.; Maia, R.C.A.P.; Rannier, L.; Andrade, L.N.; Chaud, M.V.; da Silva, C.F.; Corrêa, C.B.; de Albuquerque Junior, R.L.C.; da Costa, L.P.; Souto, E.B.; et al. Silver nanoparticles-composing alginate/gelatin hydrogel improves wound healing in vivo. Nanomaterials 2020, 10, 390. [CrossRef]
-
Hissae Yassue-Cordeiro, P.; Zandonai, C.H.; Pereira Genesi, B.; Santos Lopes, P.; Sanchez-Lopez, E.; Garcia, M.L.; Camargo Fernandes-Machado, N.R.; Severino, P.; Souto, E.B.; Ferreira da Silva, C. Development of Chitosan/Silver Sulfadiazine/Zeolite Composite Films for Wound Dressing. Pharmaceutics 2019, 11, 535. [CrossRef]
-
Severino, P.; Silveira, E.F.; Loureiro, K.; Chaud, M.V.; Antonini, D.; Lancellotti, M.; Sarmento, V.H.; da Silva, C.F.; Santana, M.H.A.; Souto, E.B. Antimicrobial activity of polymyxin-loaded solid lipid nanoparticles (PLX-SLN): Characterization of physicochemical properties and in vitro e_cacy. Eur. J. Pharm. Sci. 2017, 106, 177–184. [CrossRef]
-
Doktorovova, S.; Santos, D.L.; Costa, I.; Andreani, T.; Souto, E.B.; Silva, A.M. Cationic solid lipid nanoparticles interfere with the activity of antioxidant enzymes in hepatocellular carcinoma cells. Int. J. Pharm. 2014, 471, 18–27. [CrossRef]
-
Souto, E.B.; da Ana, R.; Souto, S.B.; Zieli ´ nska, A.; Marques, C.; Andrade, L.N.; Horba´ nczuk, O.K.; Atanasov, A.G.; Lucarini, M.; Durazzo, A.; et al. InVitro Characterization, Modelling, and Antioxidant Properties of Polyphenon-60 from Green Tea in Eudragit S100-2 Chitosan Microspheres. Nutrients 2020, 12. [CrossRef] [PubMed]
-
Giner-Casares, J.J.; Henriksen-Lacey, M.; Coronado-Puchau, M.; Liz-Marzán, L.M. Inorganic nanoparticles for biomedicine: Where materials scientists meet medical research. Mater. Today 2016, 19, 19–28. [CrossRef] Marambio-Jones, C.; Hoek, E.M. A review of the antibacterial e_ects of silver nanomaterials and potential implications for human health and the environment. J. Nanoparticle Res. 2010, 12, 1531–1551. [CrossRef]
-
Lee, J.; Mahendra, S.; Alvarez, P.J. Nanomaterials in the construction industry: A review of their applications and environmental health and safety considerations. ACS Nano 2010, 4, 3580–3590. [CrossRef] 36.Darrel R.Boverhof; Christina m. Bramante;John H. Butala;Shaun F. Cluancy;Mark Lafranconi;Jay West;Steve C. Gordon.Comparative assessment of nanomaterialdefinitions and safety evaluation considerations.Int. J. Environ.Res. Public Health 2020,17,4657.









